「その名は「H2ブロッカー」〜病気を治すロジックの誕生|世界を変えた医薬の力・後編」

Contents
前編(「その名は「H2ブロッカー」〜病気を治すロジックの誕生|世界を変えた医薬の力・前編」)に続き、医薬品開発のパラダイムを変えることになったできごとを、佐藤健太郎氏にひもといていただきます。正解がないかもしれない問いに挑んだ、そして人類史に刻まれてしかるべき、薬理学者の苦闘の物語です。
◆
前回、胃潰瘍とは胃酸の出過ぎによって自らの胃壁が消化されてしまう疾患だと述べた。多くの人がこの病気で落命したし、進行した胃潰瘍は外科手術で切除するより治療法がなかった。もし、医薬によって胃酸放出を抑えることができるなら、ずっと楽に症状を抑えることが可能になる。
切るしかない病気を、薬を飲むだけで治す。この難題に挑んだのが、英国の薬理学者ジェームズ・ブラックであった。彼はICIファーマシューティカルズ社に在籍していた1964年、狭心症や高血圧などの治療薬プロプラノロールを世に送り出したことで知られていた。
プロプラノロールは、「交感神経β受容体拮抗薬」(βブロッカー)と呼ばれるジャンルに属する薬だ。この薬は、アドレナリンの受容体に結合し、その働きをブロックしてしまう。これによって心筋の過剰な活動を抑え、狭心症を防ぐのだ。
プロプラノロールは心臓病の分野において、ジギタリス(18世紀に発見された強心剤)以来最大のブレークスルーと称され、世界で最も処方された医薬となった。何よりこの薬は、論理的な仮説に基づいて生み出された薬の第1号であり、学問的な面からも医薬品史上において燦然と輝く存在だ。
同じ手法で、胃潰瘍の治療薬も生み出せるとブラックは考えていた。しかしこの方向性は会社の方針と合わなかったため、1964年にブラックはICIを去り、スミスクライン&フレンチ社(現・グラクソ・スミスクライン)に移籍する。
胃潰瘍治療薬の突破口・ヒスタミン
ブラックが胃潰瘍治療薬の標的として考えていたのは、ヒスタミンと呼ばれる小分子であった。これが胃の受容体に結合すると、スイッチが入って胃酸が放出される。プロプラノロールの場合と同様、ヒスタミンの受容体に先回りして結合し、スイッチが入らないようブロックする化合物を投与してやれば、胃潰瘍の症状緩和が可能になるはずだ。
だがこれは、言うは易く行うは難しだ。受容体の詳しい構造は、現代でも解明不可能なことが多い。せめて、いくらかでも受容体に作用する化合物でもあれば、それを改良していくこともできたが、当時はそれすらも見つかっていなかった。何の手がかりもなしに、内部が見えない鍵穴にぴったり合う鍵を作り出せというようなものだ。
さらにヒスタミンには、もう一つ大きな謎があった。ヒスタミンの受容体をブロックする化合物は、すでに存在していた。この化合物はジフェンヒドラミンという名で、花粉症などアレルギー疾患の治療薬としても今も広く使われている。だがご存知の通り、花粉症の薬は胃潰瘍には何の効き目もない。同じヒスタミン受容体に作用するのに、なぜこうした差が生じるのだろうか?
ブラックは、ヒスタミン受容体には2種類あるという仮説を立てた。すなわち、アレルギー疾患に関与する受容体(H1受容体)と、胃酸分泌に関与する受容体(H2受容体)という、構造が異なる受容体が存在するというアイディアだ。
微妙に異なる2種類の鍵穴に対し、ヒスタミンという鍵はどちらにも結合して作用するが、ジフェンヒドラミンという鍵はH1受容体にだけ結合できる、と考えれば辻褄は合う。であるなら胃潰瘍だけを治すためには、H1受容体には結合せず、H2受容体にだけ作用する鍵を探し出せばよい。
が、理屈はそうでも、そんなものを作り出せる保証はどこにもない。もしそれが作り出せたにせよ、他の理由(体内に吸収されない、副作用を引き起こしてしまうなど)で医薬として成立しない可能性も高い。そもそも、H2受容体などというものは仮説の中の幻に過ぎないということも、十分にありうる。しかしブラックらは、このあやふやな仮説に沿って、新薬創出に挑むことを決めたのだ。
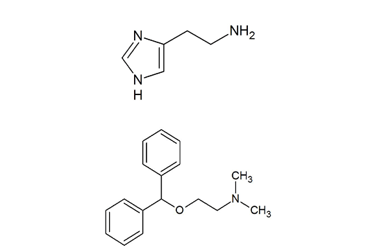
▲ヒスタミン構造式(上),ジフェンヒドラミン構造式(下)
数学の難問に、受験生が頭を絞って取り組む気になるのは、その問題に解があることが保証されているからだ。もし、この問題には解があるかないかわからないといわれたら、何時間も粘ってその問題に取り組む気には、そうそうなれないだろう。
だが、画期的新薬を創り出す過程においては、誰も「解」があるなどという保証はしてくれない。あちこちがあやふやなままでルートを立案し、登れるかどうか――いや、山頂があるかないかすらわからない登山に挑まねばならない。今も昔も創薬とはこのようなものであり、みごと山頂を制するためには、根気と知識と資金、そして幸運が不可欠だ。
筆者が現役の研究者であったころ、同ジャンルの新薬開発を競い合っていた他社に、一番乗りの座を奪われたことが何度かあった。こういう場合、もちろん悔しさもあるのだが、実はちょっとほっとするという面もある。同じタイプの新薬が認可されたということは、今自分たちが登っている道の先には、間違いなく目指す頂上があると保証されたことだからだ。
先の見えぬ戦いほど苦しいものはない。まして、遺伝子組み換え技術、X線結晶解析、コンピュータによる分子設計といった強力な武器もない時代に、研究者としてのカンだけを頼りに戦いに打って出た、ブラックの勇気には敬服する他ない。
とはいえ、H2受容体にだけ作用するなどという芸当をやってのける化合物を、いったいどこから探し出せばよいのだろうか? ブラックらが採った作戦は、H2受容体に結合することがわかっている唯一の物質――すなわちヒスタミンそのものを元に、徐々に改良していくという方法だった。ひとつひとつヒスタミンに似た化合物を合成しては、両受容体への結合力を測定する。その結果を見て、また新たな化合物をデザイン・合成するということを繰り返すのだ。
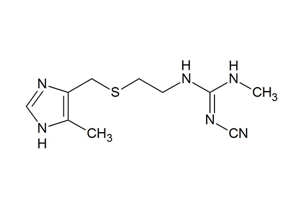
▲シメチジンの構造式
その研究過程は、多くの創薬化学の教科書に収録されているので、詳細はそちらに譲ろう。結論をいえば、ブラックらは見事H2受容体拮抗剤を創り出し、それが意図した通り胃酸の放出を抑えることを実証した。そしてこの化合物は、シメチジン(商品名タガメット)の名で1977年に市場に送り出される。研究の開始から、13年後のことであった。プロの創薬研究者なら、シメチジンの構造式を見ただけで、ここに至るまでの苦闘の積み重ねに思いを致すことができるはずだ。
「創薬」を創った男
シメチジンは、文字通りに胃潰瘍治療のパラダイムを変える医薬となった。たとえば日本では、1950年には年間19,323人が胃潰瘍及び十二指腸潰瘍のために亡くなっていたが、現在ではこの数字は3000人を切っている。もし夏目漱石の元にシメチジンを届けることができたなら、小説「明暗」が無事完結していた――のみならず、さらにいくつもの名作が彼の筆先から生まれていたことだろう。やがてシメチジンは、やはりブラックの生み出したプロプラノロールを抜き去り、世界で最も処方された医薬となった。
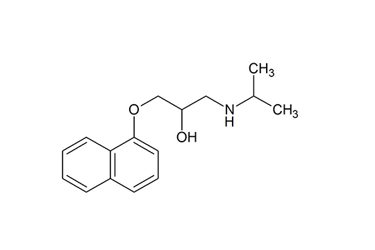
▲プロプラノロールの構造式
受容体にサブタイプがあること、スクリーニングによってそれらを「見分ける」化合物を作り出せること、ヒスタミンのような小分子をもとに医薬をデザインできること――こうした、ブラックらが確立した手法は、以後の低分子創薬のスタンダードとなった。これらの功績により、ジェームズ・ブラックは1988年のノーベル生理学・医学賞を受賞する。重要な医薬を生み出したこともさることながら、こうした現代につながる創薬の手法を確立したことが評価されたものだ。ブラックとシメチジンの名は、人類史に永遠に記念されるべきものだろう。
なお、本文中ではストレスのみを胃潰瘍の原因として描いてきたが、ヘリコバクター・ピロリと呼ばれる細菌の寄与も大きいことが後にわかっている。こちらに関する物語も、いずれ取り上げてみたい。
※本記事の内容は筆者個人の知識と経験に基づくものであり、運営元の意見を代表するものではありません。
◆
ーーーーーーーーーーーーーーーーーーーーーーーーーーーーーーーーー
佐藤健太郎さんのweb版連載「世界史を変えた薬」
その名は「H2ブロッカー」〜病気を治すロジックの誕生・前編
人類最後の敵・がんに挑む ~体内にあった最強の武器(1)
人類最後の敵・がんに挑む ~体内にあった最強の武器(2)
ーーーーーーーーーーーーーーーーーーーーーーーーーーーーーーーーー








